Chers membres et suppporters de l'ADDE, la première réunion des intervenants qui a eu lieu à Bruxelles le 23 février a été une excellente occasion de promouvoir la dentisterie européenne et de sécuriser les intérêts des professionnels dentaires et des patients, concernant les nouvelles réglementations sur les dispositifs médicaux. Différentes associations dentaires et membres ont participé à l'événement. Deux experts de l'UE ont parlé de l'impact et des résultats de la structure réglementaire.
La réunion a commencé avec une présentation des différentes associations. En tant que président, j'ai commencé par parler de l'Association des dépôts dentaires européens (ADDE). Né en 1964, l'ADDE est membre associé de la Fédération dentaire internationale (FDI), membre actif de l'Union européenne de l’artisanat et des petites et moyennes entreprises (UEAPME) et partenaire proche de la Fédération de l'industrie dentaire européenne (FIDE). L'ADDE représente les intérêts d'environ 50.000 dépôts dentaires. Nos membres sont partenaires pour offrir des solutions innovantes destinées à tous les professionnels du marché dentaire européen. L'ADDE offre des informations et des conseils sur la réglementation des dispositifs médicaux, sur les technologies nouvelles et émergentes telles que la numérisation, la numérisation intra-extral-orale, le fraisage, le frittage laser et l'impression 3D. Enfin, l'ADDE s'occupe aussi de la concurrence déloyale des entreprises qui ne respectent pas les exigences en matière de santé et de sécurité, qu'elles soient situées à l'extérieur ou à l'intérieur de l'Europe.
Fondé en 1961, le Conseil des dentistes européens (CED) représente 340.000 professionnels dentaires en Europe. Actuellement, le CED compte 29 pays membres et trois observateurs. En tant qu'organe indépendant financé par les cotisations, la mission du CED est de promouvoir un haut niveau de santé bucco-dentaire et de soins dentaires et une sécurité efficace des patients ainsi qu'une pratique professionnelle européenne. En outre, le CED favorise les intérêts de la profession dentaire et assure la protection de la santé publique. « Les patients sont au centre de notre mission. Le citoyen européen en tant que patient est notre principale préoccupation » a déclaré le Dr. Marco Landi, président du CED.
Représentant 40,000 laboratoires dentaires et 210.000 prothésistes dentaires en Europe, la Fédération internationale des prothésistes dentaires européens (Federation of European and International Dental Technicians - FEPPD) est un autre élément clé de l'industrie du commerce dentaire. Fondée en 1953, la FEPPD est passée de la représentation des fabricants à la promotion de la technologie dentaire européenne dans le monde entier. La FEPPD prend en charge les membres ayant des événements annuels, des études et des projets fondés sur l'UE. La FEPPD veut que les prothésistes dentaires fournissent des normes de sécurité des plus élevées envers les patients. Elle vise également une transparence totale de la fabrication des dispositifs dentaires. Selon le secrétaire général Pierre Zammit, la nouvelle réglementation sur les dispositifs médicaux devrait aider à fournir finalement le meilleur service au patient européen.
La Fédération de l'industrie dentaire européenne (FIDE) a été fondée en 1957 et représente les intérêts de plus de 550 fabricants dentaires. Selon le président Dr. Alessandro Gamberini, les principaux problèmes de l'industrie dentaire restent la réglementation des dispositifs médicaux, la classification du règlement 19, la capacité des organismes notifiés et l'impression en 3D. Conformément au nouveau cadre réglementaire, les nouvelles et plus strictes exigences pour l'industrie dentaire nécessiteront entre autre une évaluation clinique plus rigoureuse, des rapports techniques, un suivi clinique marqué après-vente. Il n'est toujours pas clair si la réglementation sur les dispositifs médicaux constituerait simplement un poids supplémentaire pour l'industrie et entraînerait le retrait de produits ainsi que l'insolvabilité et la fermeture de petites entreprises. Le président a également noté que le nombre d'organismes notifiés dans l'UE a diminué alors que le nombre d'audits a augmenté.
Le nouveau règlement sur les dispositifs médicaux
Le règlement des dispositifs médicaux a finalement été adopté ce mois-ci. L'application complète de la réglementation sur les dispositifs médicaux aura lieu au printemps 2020, alors que la nouvelle IVDR sera intégralement appliquée au printemps 2022. Les certificats délivrés en vertu des anciennes directives auront une durée de validité maximale de quatre ans pour les dispositifs médicaux et deux ans pour IVD après l'entrée en application. Les appareils disponibles sur le marché seront valables 5 ans pour les dispositifs médicaux et 3 ans pour la DIV.
Les deux experts de l'UE ont parlé d'un certain nombre d'avantages que le nouveau cadre fournira aux fabricants et aux revendeurs : un contrôle plus strict du marché des dispositifs à haut risque avec la participation d'experts au niveau de l'UE, l'inclusion de certains dispositifs esthétiques, une désignation renforcée et les processus de surveillance des organismes notifiés, le renforcement des règles sur l'évaluation et l'investigation clinique, des règles plus strictes pour les dispositifs «fondés sur la substance», un nouveau système de classification pour IVDS et une introduction d'un système UDI.
Les sujets ont longuement portés sur la mise en place d'une base de données européenne complète des dispositifs médicaux (EUDAMED) avec des informations publiques, la présentation de la norme à l'échelle de l'UE du soin implantaire avec des informations sur les dispositifs médicaux implantaires, un résumé de la sécurité et des résultats cliniques pour toutes les classes III et pour les dispositifs médicaux implantables et de nouvelles obligations pour les fabricants et les représentants autorisés visant à protéger les consommateurs. En outre, des questions subsistent quant à l'enregistrement des dispositifs et des opérateurs économiques, à la coordination entre les États membres et à l'évaluation coordonnée des enquêtes cliniques menées dans plus d'un État membre. Pour cela, les nouveaux systèmes EUDAMED et UDI, les organismes notifiés et la gouvernance sont les principales priorités au sein du groupe de travail de l'UE.
Des nouvelles intéressantes et des discussions controversées
Une nouveauté est que le nouveau règlement est directement applicable, ce qui signifie que le gouvernement national n'a pas à voter pour l'adopter. La loi a été restructurée pour permettre un accès plus intuitif et un système pro-actif. Le travail scientifique et les preuves cliniques sont maintenant beaucoup plus nécéssaires. Tous les fabricants, même les fabricants de classe I et les fabricants de dispositifs sur mesure devront établir une gestion des risques et de qualité. Le nombre de choix concernant l'évaluation de la conformité a été réduit de sorte que l'UE a supprimé certaines procédures. Les experts ont également mis l'accent sur la création de vérifications inopinées et d'inspections dans les entreprises. En outre, les possibilités d'étiquetage de la propre marque seront considérablement réduites lorsque des problèmes de sécurité apparaissent.
Une discussion a été soulevée quant à la question de savoir si un dentiste et un prothésiste dentaire sont des fabricants de restaurations dentaires personnalisées, ce qui signifie qu'ils doivent certifier chaque implant, bridge et autre restauration. La législation doit définir l'échelle et la limite de la personnalisation de masse afin de s'assurer que les laboratoires dentaires ne doivent pas être considérés comme des fabricants industriels. Les professionnels dentaires peuvent trouver d'autres informations sur ces sujets et d'autres, y compris sur le commerce parallèle, la surveillance du marché et la libre circulation des professionnels dentaires, dans la nouvelle étude de marché.
De plus amples informations seront disponibles dans notre prochaine newsletter. En attendant, j'aimerais inviter tout le monde à lire les autres articles et à examiner notre nouvelle enquête qui sera bientôt disponible.
Dominique Deschietere
Président
LEIPZIG, Allemagne : Fournir des informations utiles et de qualité en odontologie a toujours été un objectif principal du groupe ...
GENÈVE, Suisse : L’Organisation mondiale de la santé (OMS) a dévoilé un nouveau plan d’action mondial pour la santé bucco-dentaire, visant à ...
NEW YORK, États-Unis : La quatrième réunion de haut niveau de l’Assemblée générale des Nations Unies (AGNU) sur la prévention et la maîtrise des ...
MILAN, Italie : Les 40 membres de l'organe directeur de l’International college of dentists (ICD), le Conseil international, se sont réunis à Milan du ...
MONACO: Le 32e congrès scientifique annuel de l’Association européenne d’ostéointégration (EAO) s’est ouvert aujourd’hui au Grimaldi Forum de ...
COLOGNE, Allemagne : Avant la 35ème édition de l`International Dental Show (IDS), tous les partenaires licenciés de Dental Tribune ...
Au printemps dernier, la première réunion du conseil d'administration de la Fondation Nakao a décidé d'accorder une subvention à 6 instituts de ...
Rencontre avec le Dr Gérard Scortecci, président du congrès Euro Implanto Nice 2014
PARIS, France : L'arrivée des dents permanentes chez l’enfant est un sujet d’angoisse pour bon nombre de parents qui s’interrogent ...
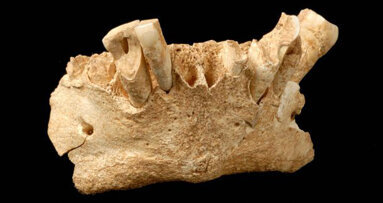
YORK, Royaume Uni/ BARCELONE, Espagne : Basée sur l’étude d’une plaque dentaire d’un hominidé, des scientifiques ont conclu que les premiers ...
Webinaire en direct
mer. le 3 juin 2026
à 19h00 (CET) Paris
Webinaire en direct
jeu. le 4 juin 2026
à 20h00 (CET) Paris
Webinaire en direct
lun. le 8 juin 2026
à 18h00 (CET) Paris
Webinaire en direct
lun. le 8 juin 2026
à 19h00 (CET) Paris
Dr. Anthony Mak B.D.S, Prof. Marleen Peumans
Webinaire en direct
lun. le 8 juin 2026
à 20h00 (CET) Paris
Webinaire en direct
mer. le 10 juin 2026
à 17h00 (CET) Paris
Webinaire en direct
mer. le 10 juin 2026
à 20h00 (CET) Paris
Nacho Fernández-Baca DDS, MSc



 Autriche / Österreich
Autriche / Österreich
 Bosnie Herzégovine / Босна и Херцеговина
Bosnie Herzégovine / Босна и Херцеговина
 Bulgarie / България
Bulgarie / България
 Croatie / Hrvatska
Croatie / Hrvatska
 République tchèque et Slovaquie / Česká republika & Slovensko
République tchèque et Slovaquie / Česká republika & Slovensko
 France / France
France / France
 Allemagne / Deutschland
Allemagne / Deutschland
 Grèce / ΕΛΛΑΔΑ
Grèce / ΕΛΛΑΔΑ
 Hongrie / Hungary
Hongrie / Hungary
 Italie / Italia
Italie / Italia
 Pays-Bas / Nederland
Pays-Bas / Nederland
 Nordique / Nordic
Nordique / Nordic
 Pologne / Polska
Pologne / Polska
 Portugal / Portugal
Portugal / Portugal
 Roumanie & Moldavie / România & Moldova
Roumanie & Moldavie / România & Moldova
 Slovénie / Slovenija
Slovénie / Slovenija
 Serbie et Monténégro / Србија и Црна Гора
Serbie et Monténégro / Србија и Црна Гора
 Espagne / España
Espagne / España
 Suisse / Schweiz
Suisse / Schweiz
 Turquie / Türkiye
Turquie / Türkiye
 Royaume-Uni et Irlande / UK & Ireland
Royaume-Uni et Irlande / UK & Ireland
 International / International
International / International
 Brésil / Brasil
Brésil / Brasil
 Canada / Canada
Canada / Canada
 Amérique latine / Latinoamérica
Amérique latine / Latinoamérica
 États-Unis / USA
États-Unis / USA
 Chine / 中国
Chine / 中国
 Inde / भारत गणराज्य
Inde / भारत गणराज्य
 Pakistan / Pākistān
Pakistan / Pākistān
 Vietnam / Việt Nam
Vietnam / Việt Nam
 ANASE / ASEAN
ANASE / ASEAN
 Israël / מְדִינַת יִשְׂרָאֵל
Israël / מְדִינַת יִשְׂרָאֵל
 Algérie, Maroc et Tunisie / الجزائر والمغرب وتونس
Algérie, Maroc et Tunisie / الجزائر والمغرب وتونس
 Moyen-Orient / Middle East
Moyen-Orient / Middle East
























































To post a reply please login or register